Biološka zdravila in podobna biološka zdravila so tako zelo zapletene strukture, da primerjava med njimi in med klasičnimi, sinteznimi kemičnimi zdravili preprosto ni mogoča. To bi bilo tako, kot če bi hoteli zmogljivost sodobnega letala primerjati z biciklom. Velika molekula kompleksnega biološkega zdravila (monoklonsko IgG1 protitelo, denimo) vsebuje tisoč aminokislin in 20 tisoč atomov. Večja molekula enostavnega biološkega zdravila – hormona trebušne slinavke, ki je v metaforični primerjavi s kolesom in letalom na ravni osebnega avtomobila – vsebuje 51 aminokislin in 788 atomov. Majhna molekula zdravila – za primer vzemimo acetilsalicilno kislino, prvo zdravilo, ki se je na trgu pojavilo v obliki tabletk, bilo že pred 115 leti zaščiteno na patentnem uradu, z imenom aspirin, in je še danes množično uporabljano – pa vsebuje pičlih 21 atomov.
Bistvena razlika:
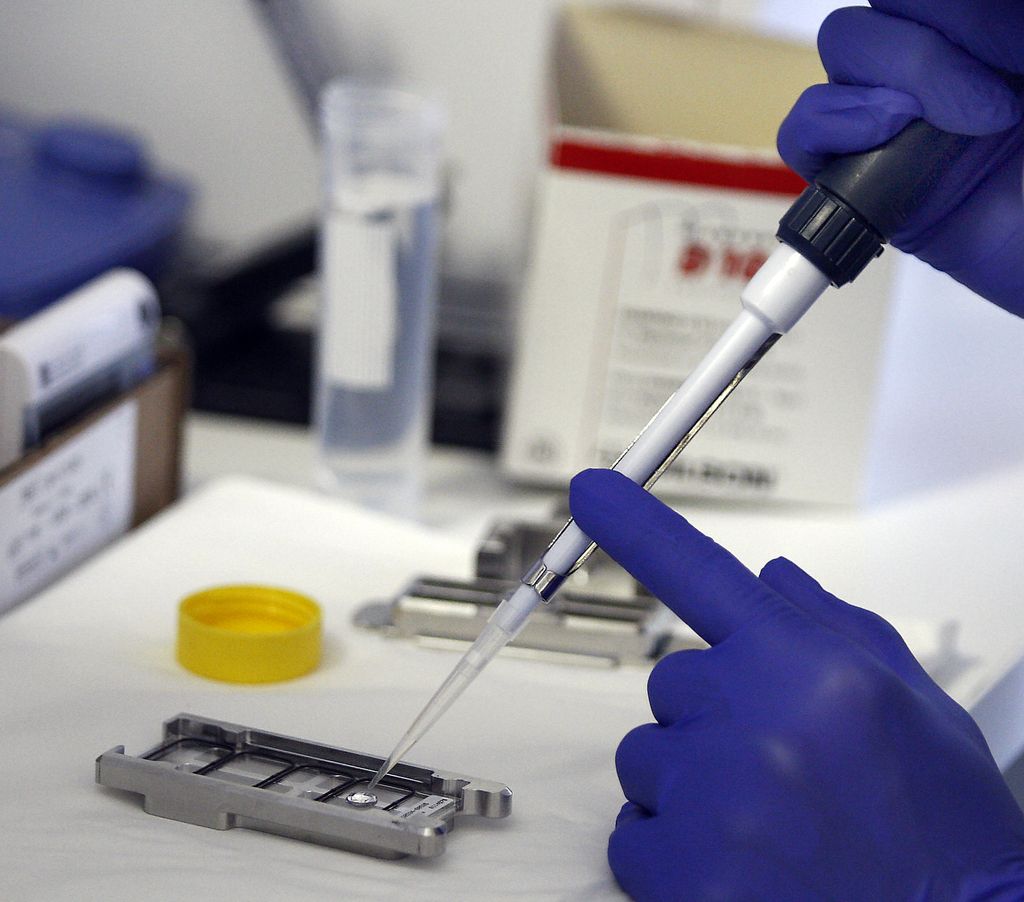
Pravzaprav ni nič nenavadnega, da je več kot polovica vseh novih zdravil, ki danes dobijo uradno zeleno luč za uporabo, pri čemer morajo ustrezati izredno strogim zahtevam glede varnosti in učinkovitosti, biološkega izvora. Za ta zdravila, pridobljena iz živih celic z biotehnološkimi postopki v zapletenem, dolgotrajnem in strogo nadzorovanem procesu izdelave, je bolj znano to, da so izredno draga. Vrtoglavi zneski, ki jih doseže zdravljenje enega samega bolnika s takšnim zdravilom, postavljajo vse zdravstvene sisteme, ne le našega, pred velikanske etične dileme. Vse se vrtijo okrog vprašanja, kako zagotoviti dovolj denarja, da bo zdravstvena blagajna lahko vsakemu bolniku, ki bi potreboval tako zdravljenje, to tudi v resnici omogočila.
Znano je, da tržni delež za biološka zdravila na svetovnem trgu na letni ravni danes znaša že približno 160 milijard evrov, medtem ko pri nas zdravljenje z biološkimi zdravili za zdaj zahteva 70 milijonov evrov na leto, pri čemer zavod za zdravstveno zavarovanje (ZZZS) kot plačnik navaja, da so se v prvem polletju tega leta v primerjavi z enakim obdobjem lani stroški za biološka zdravila povečali za 34 odstotkov. Tako v Sloveniji, denimo, zdravljenje rakavih obolenj z biološkimi zdravili na letni ravni pomeni 25-milijonski strošek, ki bi ga bilo, če bi (le) eno od teh bioloških zdravil zamenjali s podobnim biološkim zdravilom, mogoče zmanjšati za okoli dva milijona evrov na leto.
Zahtevni postopki,
Predvsem pa je znano, da teh zdravil ni mogoče natančno kopirati. To pomeni, da podobna biološka zdravila, ki prihajajo na trg, niso in ne morejo biti kopije inovativnih bioloških zdravil, saj je zdravilna učinkovina podobnega biološkega zdravila sicer zelo podobna učinkovini v originalnem zdravilu, ni pa identična. Zato morajo proizvajalci dokazati zadostno podobnost, predvsem pa varnost in učinkovitost, kar mora biti podprto tako s predkliničnimi laboratorijskimi testiranji kot s kliničnimi preizkušanji.
Pri »navadnem« zdravilu je zdravilna učinkovina generičnega zdravila kemično identična učinkovini originalnega zdravila, zato je možna medsebojna zamenljivost zdravil. Podobna biološka zdravila pa niso in ne morejo biti generiki, ker popolno kopiranje preprosto ni mogoče; čeprav se pri proizvodnji podobnega biološkega zdravila uporablja enak gen kot pri inovativnem zdravilu, na posameznih stopnjah proizvodnega procesa nastajajo razlike, ki so vse prej kot zanemarljive.
»Ne« menjavi bioloških zdravil s podobnimi
Zato mora biti pri bioloških zdravilih podobnost z referenčnim zdravilom dokazana celovito – z vidika kakovosti, učinkovitosti, biološke aktivnosti in varnosti, na podlagi obsežnih primerjalnih raziskav. Vsako tako zdravilo lahko dovoljenje za promet pridobi le po enotnem postopku.
Ta postopek teče pod okriljem evropske agencije za zdravila (EMA), ki se do medsebojne zamenljivosti teh zdravil ne opredeljuje, ampak to pristojnost prepušča vsaki državi posebej. Slovenski uradni organ na tem področju, javna agencija za zdravila in medicinske pripomočke (JAZMP), meni, da koncept medsebojne zamenljivosti – ta ima v slovenski zdravstveni sferi pri nekaterih skupinah generičnih sinteznih zdravil že nekaj časa zeleno luč, zaradi varčevalnih ukrepov in posledičnih prihrankov – za podobna biološka zdravila ni primeren.
Pa vendar bodo varčevalni prijemi prišli na vrsto tudi na tej ravni, o tem strokovnjaki na področju medicine in farmakologije ne dvomijo (več). Toda po prepričanju udeležencev nedavnega posveta o bioloških in podobnih bioloških zdravilih mora pri vseh tovrstnih spremembah presoja o uporabi zdravil, originalnih in podobnih (ta lahko pridejo na trg, ko inovativnemu biološkemu zdravilu potečejo patentne pravice), ostati v rokah zdravnika. Predvsem pa velja, tako magister farmacije prof. dr. Borut Štrukelj z ljubljanske fakultete za farmacijo, da »avtomatične zamenljivosti in uvedbe terapevtskih skupin na področju bioloških zdravil in podobnih bioloških zdravil za zdaj – oziroma dokler z leti ne bo nedvoumna dokazana varnost – ne priporočamo.«
Tudi Jure Mikolič z oddelka za zdravila ZZZS pravi, da o uvedbi mehanizma zamenljivosti na tem področju še ne razmišljajo, seveda pa pospešeno iščejo možnosti za znižanje velikanskih vsot, ki jih zahtevajo nova draga zdravila, ki prihajajo na slovenski trg. Na tej ravni bo zavod, kot kaže, dosegel konsenz s farmacevtskimi podjetji, ki stojijo za proizvodnjo teh zdravil. Ta bodo, sodeč po aktualnih napovedih, cene prilagodila in jih znižala, za okoli 20 odstotkov. Na ravni Evrope to pomeni letni prihranek približno 1,6 milijarde evrov.
 Tiskane izdaje
Tiskane izdaje