Nanotehnologija, ki nas že dolgo obkroža v vsakdanjem in delovnem okolju, se uveljavlja tudi v medicini in farmaciji. Zanimiv je razvoj sodobnih dostavnih sistemov za vnos protirakavih učinkovin na tarčna mesta v organizmu, obetavna pa je tudi nanoteranostika, to je pristop, ki združuje zdravljenje in diagnostiko.
Z načrtovanjem in pripravo nanodostavnih sistemov z ustreznimi lastnostmi glede velikosti, naboja in površine, se lahko izboljša učinkovitost zdravljenja s protirakavimi učinkovinami, hkrati pa se zmanjšajo sistemski neželeni učinki zdravil. Protirakave učinkovine je mogoče usmeriti v izbrane tarče bodisi s pasivnim ali aktivnim ciljanjem. Omejeno število nanozdravil za pasivno ciljanje rakastih tumorjev je že na voljo, nanozdravila za aktivno ciljanje pa so še v različnih fazah razvoja ali kliničnih raziskav.
Tako je dr. Petra Kocbek, mag. farm, docentka na Katedri za farmacevtsko tehnologijo Fakultete za farmacijo Univerze v Ljubljani, pred nedavnim na strokovnem posvetu internistov, predstavila možnosti, obete in aktualne raziskave, povezane s sodobnimi dostavnimi sistemi za vnos učinkovin v tarčne lezije v onkologiji. V zvezi s tem sogovornica še pojasnjuje, da so koncentracije učinkovin v tumorjih lahko nekajkrat večje v primerjavi s koncentracijami učinkovin v netarčnih tkivih, zato naj bi bilo zdravljenje učinkovitejše, neželeni učinki pa manjši. Nanodostavni sistemi zaščitijo vgrajeno učinkovino pred prehitro razgradnjo, podaljšajo njen razpolovni čas v krvnem obtoku in izboljšajo topnost težko topnih učinkovin.
Mimo ovir naravnost v tumor
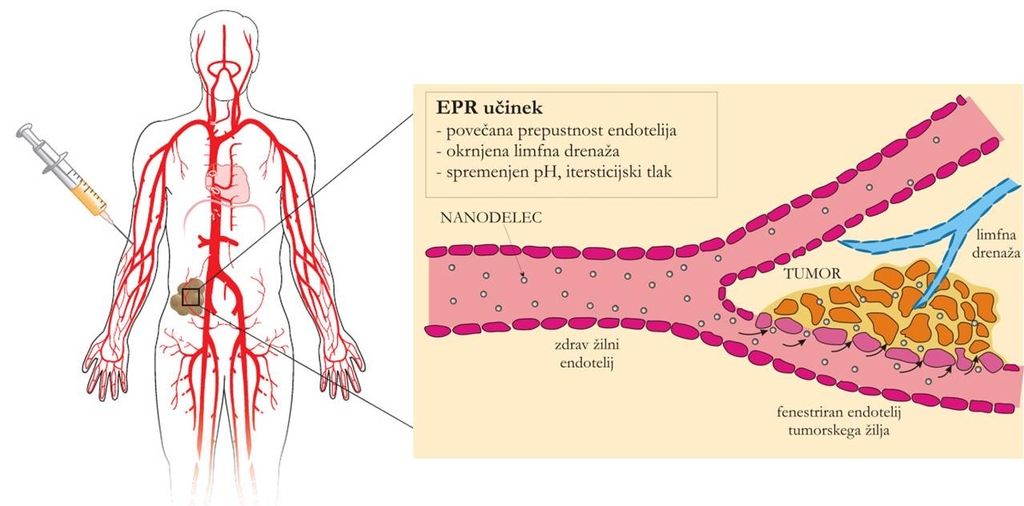
»Nadonostavni sistemi se ponavadi vnašajo v organizem intravensko, zato se morajo v krvnem obtoku zadržati dovolj dolgo, da lahko preidejo iz krvnih žil in dosežejo tarčna mesta v organizmu. Njihove lastnosti morajo biti načrtovane tako, da se izognejo oziroma premagajo fiziološke ovire in dosežejo želeno tarčno mesto, to je tumorsko žilje, tumor oziroma tarčne rakave celice.
Velikost nanodostavnih sistemov mora biti dovolj velika, da se izognejo izločanju v ledvicah, kar se zgodi, če so delčki manjši od deset nanometrov (nm). Po drugi strani pa ne smejo biti preveliki, saj v primeru nanodostavnih sistemov s hidrodinamsko velikostjo večjo od 200 nm lahko nanodostavni sistemni postanejo tarča makrofagov, ki jih prepoznajo kot tujke in odstranijo iz obtoka,« pojasnjuje doc. Petra Kocbek.
Primerno izbrana velikost nanodelcev pa je še posebno zanimiv izziv za razvoj sodobnih nanodostavnih sistemov pri zdravljenju različnih bolezenskih sprememb v možganih, kjer je zaradi znane varovalne prepreke prehod klasičnih zdravil močno oviran ali popolnoma onemogočen. Za zdaj so poskusi zdravljenja na ta način, s pomočjo nanodostavnih sistemov, povezani predvsem z rakastimi tumorji, v prihodnje pa naj bi se, kot pričakujejo, ti pristopi razširili na zdravljenje nevrodegenerativnih bolezni oziroma regenerativne medicine.
Poleg že omenjenega in za zdaj najbolj znanega intravenskega vnosa nanozdravil, raziskovalci preizkušajo še druge pristope, kot je na primer magnetna hipertermija. Doc. Kocbekova pojasnjuje, da se pri slednjem pristopu izrabi učinek izmeničnega magnetnega polja in nadzorovanega pregrevanja, kjer nato zvišana temperatura uniči na toploto občutljivejše tumorske celice.
Znana je že kar precej obsežna paleta različnih nanodostavnih sistemov, od najpreprostejših nanosuspenzij z delci učinkovine nanovelikosti, ki se že uporabljajo v klinični praksi, do zapletenejših nanodostavnih sistemov, kjer so učinkovine vezane na specifično načrtovane polimere, ki naj bi omogočale ciljano, daljše in nadzorovano delovanje zdravilne učinkovine in obnašanje nosilca v organizmu. A to so zapleteni sistemi, ki jih za zdaj v glavnem še preizkušajo.
Pasivno ali aktivno ciljanje
Nanodostavne sisteme je mogoče uporabiti za pasivno ali aktivno ciljanje tumorskih celic. Prvi pristop temelji na izkoriščanju anatomskih in patofizioloških lastnosti tumorskega mikrookolja za dostavo učinkovin v tumorje. Večina nanozdravil, ki so zdaj na voljo za zdravljenje raka, izkorišča za dostavo protirakavih učinkovin pasivno ciljanje tumorjev. Hitra rast tumorjev v zgodnjih fazah razvoja vodi v pomanjkanje hranil in kisika v njegovi sredici, zato celice odmrejo, tumor pa razvije lastno žilje, ki pa je bolj prepustno od normalnega. In prav te »ranljive točke« v novem tumorskem žilju je mogoče izrabiti za prehod visokomolekularnih učinkovin in nanosistemov iz krvnega obtoka v tumorje.
Aktivno ciljanje tumorjev pa se doseže z vezavo specifičnih ligandov, kot so na primer majhne molekule, ogljikovi hidrati, monoklonska protitelesa, peptidi, rastni dejavniki in drugo, na površini nanodostavnih sistemov z vgrajeno protirakavo učinkovino. Tak nanodostavni sistem prepozna tarčno mesto na površini tumorskih celic in se nanj selektivno veže ter sproži ustrezen učinek v celici.
Nanodostavni sistemi za aktivno ciljanje bi lahko bili precej učinkovitejši od pasivnega, vendar se kljub intenzivnim raziskavam še niso uveljavili v klinični praksi. Sogovornica razlaga, da so razlogi za to verjetno v različnih barierah, ki jih mora nanodostavni sistem po vnosu v organizem preiti, da doseže tarčno celico in stopi vanjo. Učinke tega pristopa pa zmanjšuje tudi povečana imunogenost nanodostavnih sistemov za aktivno ciljanje.
Predpisi ne dohajajo novosti
Veliko opisanih pristopov je videti obetavnih, vendar jih za zdaj preizkušajo v glavnem na živalskih modelih. Sogovornica pravi, da je razvoj nanodostavnih sistemov, novih materialov in pristopov sicer tako hiter, da jih zakonodaja preprosto ne dohaja. In ker torej še ni na voljo dovolj zanesljivih nadzornih mehanizmov za preverjanje in dokazovanje varnosti in učinkovitosti vseh, tudi najsodobnejših nanodostavnih sistemov, se ti uveljavljajo počasneje od pričakovanj.
Z nevidnimi »kočijaži« naravnost do tumorja
Nanodostavni sistemi - Prihodnost tudi za inovativna in generična zdravila?
Objavljeno
09. oktober 2015 19.13
 Tiskane izdaje
Tiskane izdaje